Autor:
Helen Garcia
Data E Krijimit:
21 Prill 2021
Datën E Azhurnimit:
1 Korrik 2024
Përmbajtje
Një ekuacion kimik është një përfaqësim simbolik i një reaksioni kimik. Në këtë rast, komponimet reaguese (reagentët) shkruhen në të majtë, dhe substancat që rezultojnë (produktet e reagimit) - në anën e djathtë të ekuacionit. Një shigjetë vendoset midis tyre nga e majta në të djathtë, e cila tregon drejtimin e reagimit. Sipas ligjit të ruajtjes së masës, gjatë një reaksioni kimik, atomet e rinj nuk mund të shfaqen ose ato të vjetra të zhduken; prandaj, numri i atomeve në reagentët duhet të jetë i barabartë me numrin e atomeve në produktet e reaksionit kimik Me Ky artikull përshkruan se si të balanconi ekuacionet kimike duke përdorur metoda të ndryshme.
Hapa
Metoda 1 nga 2: Metoda Tradicionale
 1 Shkruani një ekuacion kimik. Si shembull, merrni parasysh reagimin e mëposhtëm:
1 Shkruani një ekuacion kimik. Si shembull, merrni parasysh reagimin e mëposhtëm: - C3H8 + O2 -> H2O + CO2
- Ky reagim përshkruan djegien e propanit (C3H8) në prani të oksigjenit për të formuar ujë dhe dioksid karboni (dioksid karboni).
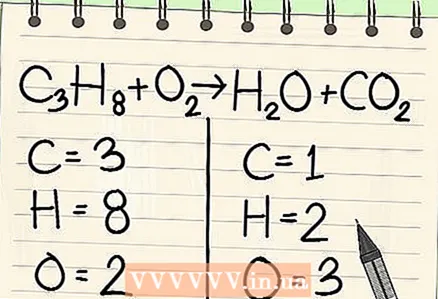 2 Shkruani numrin e atomeve për secilin element. Bëni këtë për të dy anët e ekuacionit. Vini re nënshkrimet pranë secilit element për të përcaktuar numrin e përgjithshëm të atomeve. Shkruani simbolin për secilin element në ekuacion dhe shënoni numrin përkatës të atomeve.
2 Shkruani numrin e atomeve për secilin element. Bëni këtë për të dy anët e ekuacionit. Vini re nënshkrimet pranë secilit element për të përcaktuar numrin e përgjithshëm të atomeve. Shkruani simbolin për secilin element në ekuacion dhe shënoni numrin përkatës të atomeve. - Për shembull, në anën e djathtë të ekuacionit në shqyrtim, si rezultat i shtimit, marrim 3 atome oksigjeni.
- Në anën e majtë, ne kemi 3 atome karboni (C3), 8 atome hidrogjeni (H8) dhe 2 atome oksigjeni (O2).
- Në anën e djathtë kemi 1 atom karboni (C), 2 atome hidrogjeni (H2) dhe 3 atome oksigjeni (O + O2).
 3 Kurseni hidrogjenin dhe oksigjenin për më vonë, pasi ato janë pjesë e disa përbërjeve në anën e majtë dhe të djathtë. Hidrogjeni dhe oksigjeni janë pjesë e disa molekulave, prandaj është mirë që ato të balancohen të fundit.
3 Kurseni hidrogjenin dhe oksigjenin për më vonë, pasi ato janë pjesë e disa përbërjeve në anën e majtë dhe të djathtë. Hidrogjeni dhe oksigjeni janë pjesë e disa molekulave, prandaj është mirë që ato të balancohen të fundit. - Para balancimit të hidrogjenit dhe oksigjenit, do t'ju duhet të rillogarisni atomet përsëri, pasi faktorë shtesë mund të jenë të nevojshëm për të balancuar elementët e tjerë.
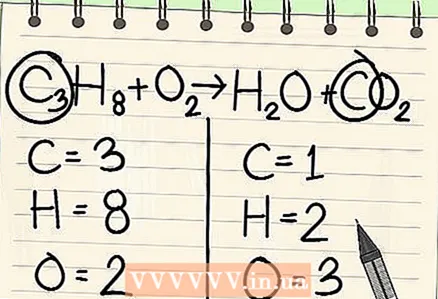 4 Filloni me artikullin më pak të shpeshtë. Nëse keni nevojë të balanconi disa elementë, zgjidhni një që është pjesë e një molekule reagenti dhe një molekule të produkteve të reagimit. Pra, karboni duhet së pari të balancohet.
4 Filloni me artikullin më pak të shpeshtë. Nëse keni nevojë të balanconi disa elementë, zgjidhni një që është pjesë e një molekule reagenti dhe një molekule të produkteve të reagimit. Pra, karboni duhet së pari të balancohet. 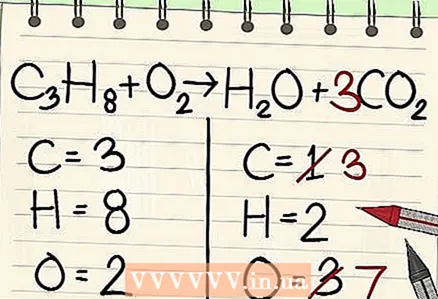 5 Për ekuilibër, shtoni një faktor para një atomi të vetëm të karbonit. Vendosni një faktor para karbonit të vetëm në anën e djathtë të ekuacionit për ta balancuar atë me 3 karbone në anën e majtë.
5 Për ekuilibër, shtoni një faktor para një atomi të vetëm të karbonit. Vendosni një faktor para karbonit të vetëm në anën e djathtë të ekuacionit për ta balancuar atë me 3 karbone në anën e majtë. - C3H8 + O2 -> H2O + 3CO2
- Një faktor 3 para karbonit në anën e djathtë të ekuacionit tregon se ka tre atome karboni, të cilat korrespondojnë me tre atomet e karbonit në molekulën e propanit në anën e majtë.
- Në një ekuacion kimik, ju mund të ndryshoni koeficientët para atomeve dhe molekulave, por nënshkrimet duhet të mbeten të pandryshuara.
 6 Pastaj balanconi atomet e hidrogjenit. Pasi të keni barazuar numrin e atomeve të karbonit në anën e majtë dhe të djathtë, hidrogjeni dhe oksigjeni mbetën të pabalancuar. Ana e majtë e ekuacionit përmban 8 atome hidrogjeni, i njëjti numër duhet të jetë në të djathtë. Arriteni këtë me një raport.
6 Pastaj balanconi atomet e hidrogjenit. Pasi të keni barazuar numrin e atomeve të karbonit në anën e majtë dhe të djathtë, hidrogjeni dhe oksigjeni mbetën të pabalancuar. Ana e majtë e ekuacionit përmban 8 atome hidrogjeni, i njëjti numër duhet të jetë në të djathtë. Arriteni këtë me një raport. - C3H8 + O2 -> 4H2O + 3CO2
- Ne kemi shtuar një faktor 4 në të djathtë, pasi nënshkrimi tregon se ne tashmë kemi dy atome hidrogjeni.
- Nëse shumëzoni faktorin 4 me nënshkrimin 2, merrni 8.
- Si rezultat, 10 atome oksigjeni merren në anën e djathtë: 3x2 = 6 atome në tre molekula 3CO2 dhe katër atome të tjerë në katër molekula uji.
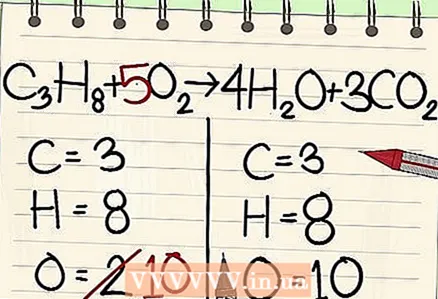 7 Balanconi atomet e oksigjenit. Mos harroni të merrni parasysh faktorët që keni përdorur për të balancuar atomet e tjerë. Për shkak se keni shtuar koeficientët para molekulave në anën e djathtë të ekuacionit, numri i atomeve të oksigjenit ndryshoi. Tani keni 4 atome oksigjeni në molekulat e ujit dhe 6 atome oksigjeni në molekulat e dioksidit të karbonit. Kështu, ka 10 atome oksigjeni në anën e djathtë.
7 Balanconi atomet e oksigjenit. Mos harroni të merrni parasysh faktorët që keni përdorur për të balancuar atomet e tjerë. Për shkak se keni shtuar koeficientët para molekulave në anën e djathtë të ekuacionit, numri i atomeve të oksigjenit ndryshoi. Tani keni 4 atome oksigjeni në molekulat e ujit dhe 6 atome oksigjeni në molekulat e dioksidit të karbonit. Kështu, ka 10 atome oksigjeni në anën e djathtë. - Shtoni një faktor 5 në molekulën e oksigjenit në anën e majtë të ekuacionit. Çdo pjesë tani përmban 10 atome oksigjeni.
- C3H8 + 5O2 -> 4H2O + 3CO2.

- Pra, të dy anët e ekuacionit përmbajnë të njëjtin numër të atomeve të karbonit, hidrogjenit dhe oksigjenit. Ekuacioni është i balancuar.
Metoda 2 nga 2: Metoda algjebrike
- 1 Shkruani ekuacionin e reaksionit. Si shembull, merrni parasysh reagimin kimik të mëposhtëm:
- PCl5 + H2O -> H3PO4 + HCl
- 2 Vendosni një shkronjë para secilës lidhje:
- aPCl5 + bH2O -> cH3PO4 + dHCl
- 3 Barazoni numrin e atomeve për secilin element në anën e majtë dhe të djathtë të ekuacionit.
- aPCl5 + bH2O -> cH3PO4 + dHCl
- Në të majtë kemi 2b atomet e hidrogjenit (2 në secilin H2O), ndërsa në të djathtë është 3c+d atomet e hidrogjenit (3 në secilin H3PO4 dhe 1 në secilën molekulë HCl). Meqenëse anët e majta dhe të djathta duhet të përmbajnë të njëjtin numër të atomeve të hidrogjenit, 2b duhet të jetë e barabartë me 3c+d.
- Bëni këtë për të gjithë elementët:
- P: a=c
- Cl: 5a=d
- H: 2b=3c+d
- 4 Zgjidhni sistemin e ekuacioneve për të gjetur vlerat numerike të koeficientëve. Sistemi ka disa zgjidhje, pasi ka më shumë ndryshore sesa ekuacione. Necessaryshtë e nevojshme të gjendet një zgjidhje e tillë në mënyrë që të gjithë koeficientët të kenë formën e numrave të plotë më të vegjël të mundshëm.
- Për të zgjidhur shpejt një sistem ekuacionesh, caktoni një vlerë numerike njërit prej ndryshoreve. Supozoni a = 1. Le të zgjidhim sistemin dhe të gjejmë vlerat e ndryshoreve të mbetura:
- Për P a = c, kështu c = 1
- Për Cl 5a = d, pra d = 5
- Meqenëse për H 2b = 3c + d, gjejmë vlerën b:
- 2b = 3 (1) + 5
- 2b = 3 + 5
- 2b = 8
- b = 4
- Kështu, ne kemi koeficientët e mëposhtëm:
- a = 1
- b = 4
- c = 1
- d = 5
Këshilla
- Nëse keni vështirësi, një kalkulator online mund të përdoret për të balancuar ekuacionet kimike. Ju lutemi vini re, megjithatë, se një kalkulator i tillë nuk lejohet të përdoret gjatë provimit, kështu që mos u mbështetni vetëm në të.
- Mos harroni, ndonjëherë ekuacioni mund të thjeshtohet! Nëse të gjithë koeficientët ndahen edhe me një numër të plotë, thjeshtoni ekuacionin.
Paralajmërimet
- Për të hequr qafe koeficientët thyesorë, shumëzoni të gjithë ekuacionin (anët e tij të majtë dhe të djathtë) me emëruesin e thyesës.
- Asnjëherë mos përdorni thyesa si koeficientë të ekuacionit kimik - nuk ka gjysmë molekula ose atome në reaksionet kimike.
- Në procesin e balancimit, mund të përdorni thyesa për lehtësi, por ekuacioni nuk është i balancuar për aq kohë sa ka koeficientë të pjesshëm në të.