Autor:
Monica Porter
Data E Krijimit:
22 Marsh 2021
Datën E Azhurnimit:
1 Korrik 2024
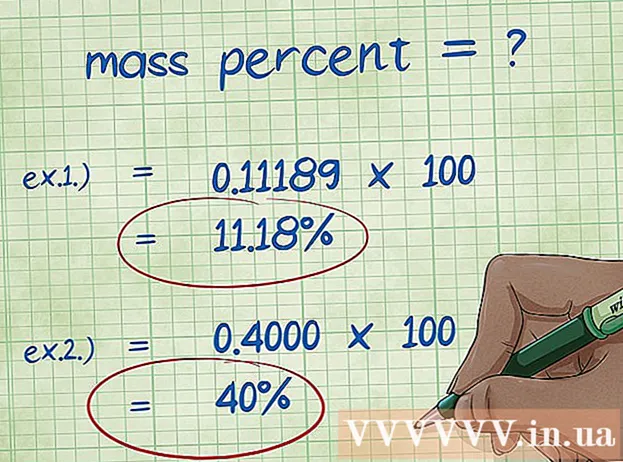
Përmbajtje
Përqindja e masës tregon përqindjen e secilit element në një përbërje kimike. Për të gjetur përqindjen e masës, duhet njohur masa molare e elementeve në përbërje në gram / mol ose numri i gramëve të substancave që përbëjnë tretësirën. Përqindja e masës llogaritet duke përdorur një formulë të thjeshtë që ndan masën e elementit (ose tretësirës) me masën e përbërjes (ose tretësirës).
Hapat
Metoda 1 nga 2: Llogaritni përqindjen e masës duke ditur masën
Përcaktoni ekuacionin për përqindjen e masës në përzierje. Formula themelore për llogaritjen e përqindjes së masës në përzierje është: përqindja e masës = (masë cilësore / masë e përzier) x 100. Më në fund duhet të shumëzoni me 100 për të përfaqësuar përqindjen.
- Shkruani një ekuacion kur filloni të zgjidhni problemin: përqindja e masës = (masa e substancës / masa e përzier) x 100.
- Sasia e cilësisë do të jepet në problem. Nëse tema nuk është dhënë, atëherë referojuni seksionit vijues se si të gjeni përqindjet e masës pa ditur peshat.
- Masa e përzierjes është e barabartë me masën totale të substancave që përbëjnë përzierjen ose tretësirën.

Llogaritni masën e përzierjes. Pasi të njihni masat e elementeve ose përbërjeve, gjithçka që duhet të bëni është t'i shtoni ato për të marrë masën e përzierjes përfundimtare ose tretësirës. Ky është emëruesi në formulën për masën e përqindjes.- Shembulli 1: Sa është përqindja në masë e 5 g hidroksid natriumi kur tretet me 100g ujë?
- Masa e përzierjes është masa totale e hidroksidit të natriumit dhe ujit: 100g + 5g. Pra, pesha e përzier është 105g.
- Shembulli 2: Cila masë e klorurit të natriumit dhe ujit kërkohet për të formuar 175g një solucion 15%?
- Në këtë shembull, ku e dini masën e përzier dhe përqindjen e masës, detyra kërkon të gjejë masën e tretësirës së shtuar. Masa e përzierjes është 175 g.
- Shembulli 1: Sa është përqindja në masë e 5 g hidroksid natriumi kur tretet me 100g ujë?

Përcaktoni masën e substancës për të gjetur masën e përqindjes. Kur kuizi kërkon të gjejë "përqindjen e masës" të një substance, duhet të gjesh masën e substancës si përqindje e masës totale të të gjithë përbërësve. Shkruani masën e substancës për të gjetur masën e përqindjes. Ky është numëruesi në formulën për masën e përqindjes.- Shembull 1: Masa e hidroksidit të natriumit (substanca që do të gjendet nga fraksioni masiv) është 5g.
- Shembulli 2: Në këtë shembull, sasia e substancës po kërkon përqindjen e masës së panjohur, dhe ju po e kërkoni atë.

Zëvendëso ndryshoret me ekuacionin e përqindjeve të masës. Pasi të keni përcaktuar vlerën e secilës ndryshore, thjesht futini ato në ekuacion.- Shembulli 1: përqindja e masës = (masa e substancës / masa e përzier) x 100 = (5 g / 105 g) x 100.
- Shembulli 2: Duhet të konvertojmë ekuacionin e përqindjes së masës për të llogaritur sasinë e cilësisë së panjohur: masa e cilësisë = (përqindja e masës * masa e përzier) / 100 = (15 * 175) / 100 .
Llogaritni përqindjen e vëllimit. Tani që ekuacioni është mbushur, duhet të llogaritni vetëm përqindjen e masës. Ndani masën e substancës me masën e përzierjes, pastaj shumëzojeni atë me 100. Kjo është përqindja e masës së substancës në përzierje.
- Shembull 1: (5/105) x 100 = 0,04761 x 100 = 4,761%. Kështu përqindja në masë e 5 g hidroksid natriumi të tretur në 100g ujë është 4,761%.
- Shembulli 2: Ekuacioni pas konvertimit për të llogaritur sasinë e cilësisë është (masa e përqindjes * pesha e përzier) / 100: (15 * 175) / 100 = (2625) / 100 = 26,25 gram klorid sodium.
- Pesha e ujit të shtuar është masa e përzierjes minus peshën e substancës: 175 - 26.25 = 148.75 gram ujë.
Metoda 2 e 2: Llogaritni përqindjen e masës kur masa është e panjohur
Përcaktoni ekuacionin për përqindjen e masës në përbërje. Formula themelore për llogaritjen e përqindjes së masës në një përbërje është: përqindja e masës = (masa molar thelbësore / masa molare e përbërësit) x 100. Masa molar thelbësore është masa e një moli të elementit ndërsa masa molekulare është masa e një moli të përbërjes. Më në fund, duhet të shumëzoni me 100 për të marrë vlerën e përqindjes.
- Shkruani një ekuacion kur filloni të zgjidhni problemin: përqindja e masës = (masa molar thelbësore / masa molare e përbërjes) x 100.
- Njësitë e dy vlerave të mësipërme janë gram për mol (g / mol).
- Kur problemi nuk jep masë, mund të përdorni masën molare për të llogaritur përqindjen e masës së elementit.
- Shembulli 1: Llogaritni përqindjen e masës së hidrogjenit në një molekulë uji.
- Shembulli 2: Llogaritni përqindjen në masë të karbonit në një molekulë glukoze.
Shkruaj Formula kimike. Nëse problemi nuk mbulon formulat kimike për secilën përbërje, do t'ju duhet t'i shkruani ato. Nëse problemi është për formulën kimike, kaloni këtë hap dhe shkoni te hapi "Gjeni masën e secilit element".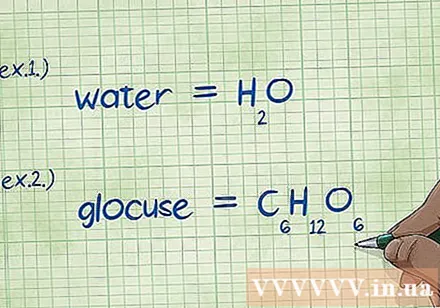
- Shembull 1: Shkruani formulën kimike për ujë, H2O.
- Shembulli 2: Shkruani formulën kimike të glukozës, C6H12O6.
Gjeni masën e secilit element në përbërje. Shikoni peshën molekulare të secilit element në formulën kimike në sistemin periodik. Masa elementare zakonisht shkruhet nën simbolin kimik. Shkruani masën e secilit element në përbërje.
- Shembulli 1: Mund të zbulojmë se atomi i masës së oksigjenit është 15,9994; dhe atomi kub i hidrogjenit është 1.0079.
- Shembulli 2: Gjetëm se atomi i masës së karbonit është 12,0107; oksigjeni është 15,9994; dhe hidrogjeni është 1.0079.
Shumëzoni atomin kub me raportin molar. Përcaktoni numrin e moleve (raporti molar) të secilit element në përbërjen kimike. Raporti molar llogaritet nga numri i vogël më poshtë në formulën kimike të përbërjes. Shumëzoni atomin kub të secilit element me raportin molar.
- Shembull 1: Hidrogjeni ka një nënshkrim prej dy ndërsa oksigjeni ka një nënshkrim prej 1. Pra shumëzoni peshën molekulare të hidrogjenit me 2, 1,00794 X 2 = 2,01588; dhe masa molekulare e oksigjenit është 15,9994 (shumëzuar me një).
- Shembulli 2: Karboni ka një nënshkrim prej 6, hidrogjeni është 12 dhe oksigjeni është 6. Shumëzoni atomin kub të secilit element me indeksin më poshtë.
- Karbon (12,0107 * 6) = 72,0642
- Hidrogjen (1,00794 * 12) = 12,09528
- Oksigjen (15,9994 * 6) = 95,9964
Llogaritni masën totale të përbërjes. Shtoni masat e të gjithë elementëve në përbërje. Ju mund të llogaritni masën totale të përbërjeve duke përdorur masat e llogaritura si raporte molare. Ky numër do të jetë emëruesi në ekuacionin masiv të përqindjes.
- Shembulli 1: Shtoni 2,01588 g / mol (masa e dy moleve të atomeve të hidrogjenit) në 15,9994 g / mol (masa e një mol atome oksigjeni) jep 18,01528 g / mol.
- Shembulli 2: Shtoni të gjitha peshat së bashku: karbon + hidrogjen + oksigjen = 72,0642 + 12,09528 + 95,9964 = 180,156 g / mol.
Përcaktoni masën elementare në të cilën do të llogaritet përqindja e masës. Kur problemi kërkon "përqindjen e masës", kjo do të thotë që duhet të gjesh masën e një elementi të veçantë në përbërje si përqindje e masës totale të të gjithë elementëve. Përcaktoni dhe shkruani masën e elementit. Kjo masë është masa e shprehur në raport molar. Ky numër është numëruesi i ekuacionit të përqindjes së masës.
- Shembull 1: Masa e hidrogjenit në një përbërje është 2.01588 g / mol (masa e dy moleve të atomeve të hidrogjenit).
- Shembulli 2: Masa e karbonit në një përbërje është 72.0642 g / mol (masa e gjashtë moleve të atomeve të karbonit).
Zëvendëso ndryshoret me ekuacionin e përqindjeve të masës. Pas përcaktimit të vlerave të secilës ndryshore, thjesht zëvendësojini ato me ekuacionin e identifikuar në hapin e parë: masa e përqindjes = (masa molar thelbësore / masa molare e përbërjes) x 100 .
- Shembulli 1: përqindja e masës = (masa molar elementare / masa molar e përbërjes) x 100 = (2,1588 / 18,1528) x 100.
- Shembulli 2: përqindja e masës = (masa molare thelbësore / masa molare e përbërësit) x 100 = (72,0642 / 180,156) x 100.
Llogaritni përqindjen e vëllimit. Tani që ekuacioni është mbushur, duhet të llogaritni vetëm përqindjen e masës. Ndani masën e elementit me masën totale të përbërjes, pastaj shumëzojeni atë me 100. Kjo është përqindja e masës së elementit në përbërje.
- Shembull 1: përqindja e masës = (2,01588 / 18,01528) x 100 = 0,111189 x 100 = 11,18%. Kështu, përqindja e masës së atomit të hidrogjenit në molekulën e ujit është 11.18%.
- Shembulli 2: përqindja e masës = (masa molarë elementare / masa molare e përbërësit) x 100 = (72,0642 / 180,156) x 100 = 0,4000 x 100 = 40,00%. Pra, përqindja e masës së atomit të karbonit në molekulën e glukozës është 40.00%.