Autor:
Lewis Jackson
Data E Krijimit:
12 Mund 2021
Datën E Azhurnimit:
1 Korrik 2024
Përmbajtje
Përcaktimi i numrit të neutroneve në një atom është mjaft i thjeshtë, madje as nuk keni nevojë të bëni ndonjë eksperiment. Për të llogaritur numrin e neutroneve në një atom normal ose izotop, thjesht duhet të keni gati një tryezë periodike dhe të ndiqni udhëzimet.
Hapat
Metoda 1 nga 2: Gjeni numrin e neutroneve në një atom normal
Përcaktoni pozicionin e elementit në sistemin periodik. Për shembull, ne do të gjejmë elementin osmium (Os) në rreshtin e gjashtë nga maja.
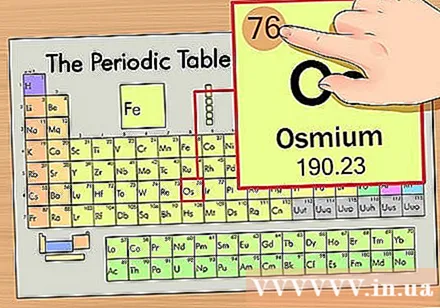
Gjeni numrin atomik të elementit. Ky është numri më i dukshëm që shkon nga secili element dhe është mbi simbolin kryesor (në tabelën që po përdorim nuk ka numra të tjerë). Numri atomik është numri i protoneve në një atom të vetëm të këtij elementi. Os është numri 76, që do të thotë se ka 76 protone në një atom osmium.- Numri i protoneve nuk ndryshon kurrë në një element; në thelb është karakteristika përcaktuese e një elementi.
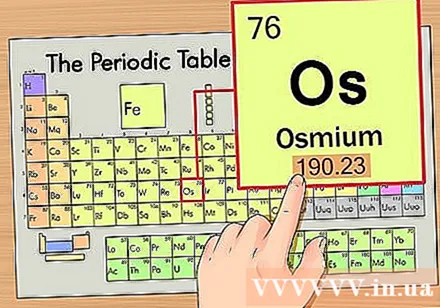
Gjeni peshën atomike të elementit. Ky numër zakonisht gjendet poshtë simbolit kryesor. Vini re se tabela periodike në këtë shembull ka vetëm numër atomik dhe pa peshë atomike. Jo të gjitha tabelat periodike. Osmiumi ka një peshë atomike prej 190.23.
Raundin e peshës atomike në numrin e plotë më të afërt për të marrë masën atomike. Për shembull, 190.23 do të rrumbullakoset në 190, kështu që masa atomike e osmiumit është 190.- Pesha atomike është mesatarja e izotopeve të të njëjtit element kimik, prandaj zakonisht nuk është një numër i plotë.
Zbrit numrin atomik nga masa atomike. Meqenëse shumica e masës atomike është masa e protoneve dhe neutroneve, duke zbritur numrin e protoneve nga masa atomike (d.m.th., numri atomik) ju do të numëroj merrni numrin e neutroneve në atom. Numri pas pikës dhjetore paraqet masën shumë të vogël të elektroneve në atom. Në këtë shembull, kemi: 190 (atom në masë) - 76 (numri i protoneve) = 114 (numri i neutroneve).
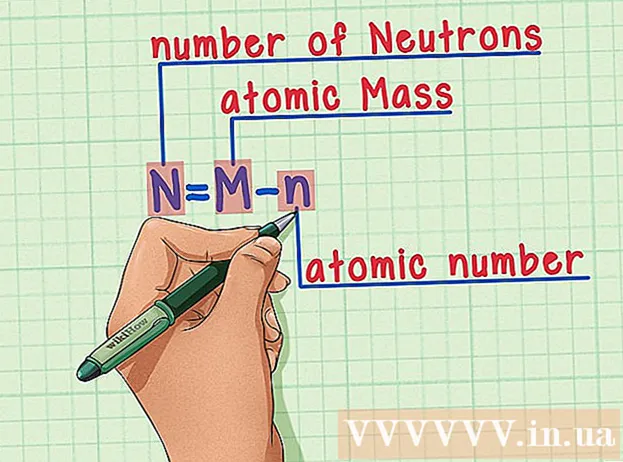
Mësuar përmendësh recetën. Për të gjetur numrin e neutroneve, ne thjesht përdorim formulën e mëposhtme: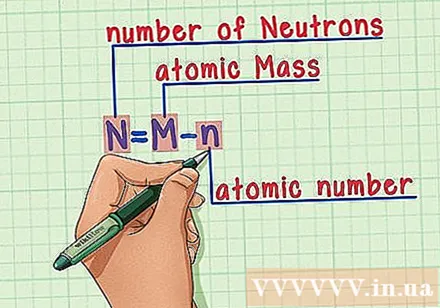
- N = M - n
- N = numri i neutroneve
- M = masë atomike
- n = numri atomik
- N = M - n
Metoda 2 nga 2: Gjeni numrin e neutroneve në izotop
Përcaktoni pozicionin e elementit në sistemin periodik. Le të marrim si shembull elementin izotop karbon-14. Meqenëse forma izotop e karbonit-14 është thjesht karboni (C), kërkoni karbon në tryezën periodike (rreshti i dytë nga lart).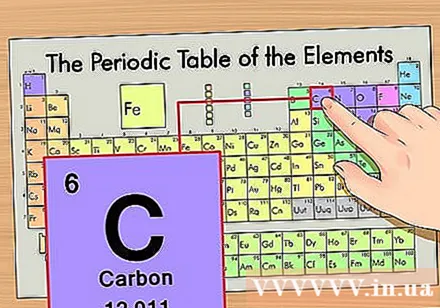
Gjeni numrin atomik të elementit. Ky është numri më i dukshëm që shkon nga secili element dhe është mbi simbolin kryesor (në tabelën që po përdorim nuk ka numra të tjerë). Numri atomik është numri i protoneve në një atom të vetëm të këtij elementi. C është numri 6, që do të thotë se ka 6 protone në një atom karboni.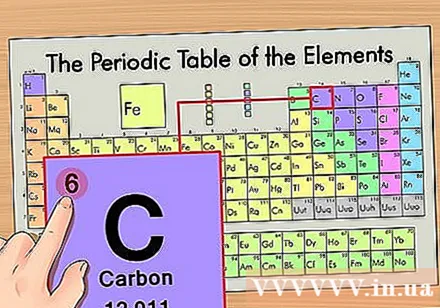
Gjeni masën atomike. Kjo është jashtëzakonisht e lehtë me izotopet sepse ata janë emëruar pas masës atomike. Për shembull, karboni-14 do të kishte një masë atomike prej 14. Pasi të keni gjetur masën atomike të izotopit, hapat e mbetur për gjetjen e numrit të neutroneve do të jenë të njëjta me atë të një atomi normal.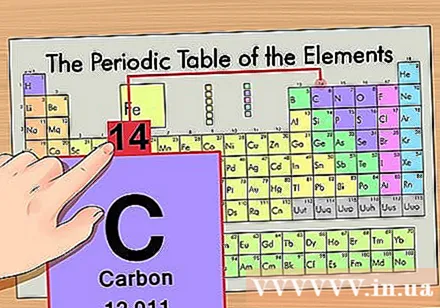
Zbrit numrin atomik nga masa atomike. Meqenëse shumica e masës atomike është masa e protoneve dhe neutroneve, duke zbritur numrin e protoneve nga masa atomike (d.m.th., numri atomik) ju do të numëroj merrni numrin e neutroneve në atom. Numri pas pikës dhjetore paraqet masën shumë të vogël të elektroneve në atom. Në këtë shembull, kemi: 14 (atom në masë) - 6 (numri i protoneve) = 8 (numri i neutroneve).
Mësuar përmendësh recetën. Për të gjetur numrin e neutroneve, ne aplikojmë formulën e mëposhtme: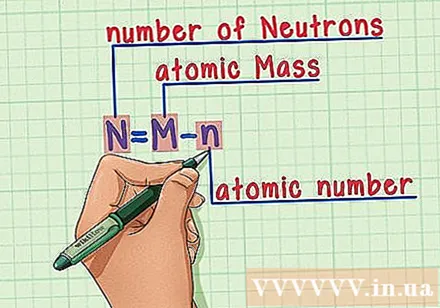
- N = M - n
- N = numri i neutroneve
- M = masë atomike
- n = numri atomik
- N = M - n
Këshilla
- Masa e një elementi është kryesisht masa e protoneve dhe neutroneve, ndërsa masat e elektroneve dhe elementëve të tjerë janë të papërfillshme (afër zeros). Meqenëse masa e protonit është përafërsisht e barabartë me masën e neutronit, dhe numri atomik paraqet numrin e protoneve, ne duhet vetëm të zbresim numrin e protoneve nga masa totale.
- Nëse nuk e mbani mend kuptimin e numrave në tabelën periodike, mos harroni se tabela periodike zakonisht ndërtohet në numra atomikë (d.m.th. numri i protoneve), duke filluar nga 1 (hidrogjen) dhe duke rritur një njësi nga majtas djathtas, duke përfunduar me 118 (ununoctium). Meqenëse numri i protoneve është një tipar identifikues i secilit atom, ajo është vetia më e thjeshtë mbi të cilën janë rregulluar elementet. (Për shembull, një atom me 2 protone është gjithmonë helium, ashtu si një atom me 79 protone është gjithmonë ari.)
Burimet dhe citimet
- Tabela periodike interaktive